Dekan – właściwości chemiczne, zastosowanie i znaczenie w chemii organicznej
Budowa i właściwości fizykochemiczne dekanu
Wzór sumaryczny i strukturalny dekanu
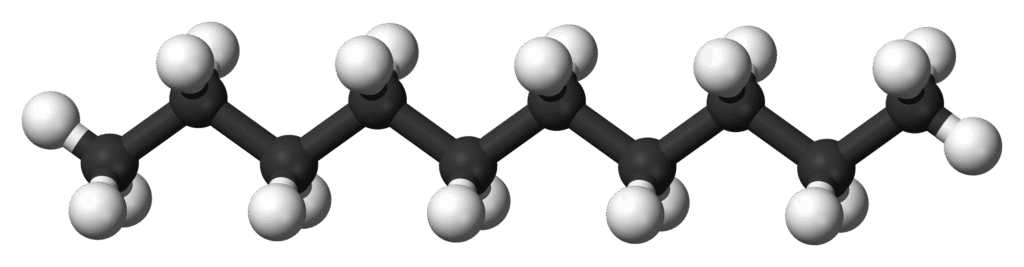
Dekan to jeden z prostszych przedstawicieli grupy alkanów, czyli nasyconych węglowodorów zawierających wyłącznie wiązania pojedyncze między atomami węgla. Jego wzór sumaryczny to C₁₀H₂₂, co oznacza, że cząsteczka dekanu składa się z dziesięciu atomów węgla i dwudziestu dwóch atomów wodoru. Jest to związek należący do szeregu homologicznego alkanów, znajdujący się między nonanem (C₉H₂₀) a undekanem (C₁₁H₂₄).
Pod względem struktury dekan może występować w różnych izomerach konstytucyjnych – najprostszym z nich jest n-dekan, czyli łańcuch prosty, w którym wszystkie atomy węgla są połączone liniowo. Poza nim istnieje wiele izomerów rozgałęzionych, takich jak 2-metylononan, 3-metylononan, 4,5-dimetylooktan i inne, które różnią się rozmieszczeniem grup alkilowych, ale mają ten sam wzór sumaryczny. W chemii organicznej izomery dekanu są ważne, ponieważ wykazują nieco odmienne właściwości fizyczne i chemiczne, mimo identycznego składu atomowego.
Budowa n-dekanu jest przykładem struktury hydrofobowej, pozbawionej jakichkolwiek grup funkcyjnych zdolnych do tworzenia wiązań wodorowych lub reagowania w warunkach typowych dla chemii kwasowo-zasadowej. To sprawia, że dekan jest bardzo stabilny chemicznie, ma niską reaktywność i zachowuje się obojętnie w większości środowisk.
Właściwości fizyczne: temperatura wrzenia, stan skupienia, palność
Dekan w warunkach standardowych (25°C, 1 atm) jest bezbarwną, oleistą cieczą o charakterystycznym zapachu przypominającym benzynę. Należy do grupy cieczy o wysokiej temperaturze wrzenia, wynoszącej około 174°C, co oznacza, że paruje znacznie wolniej niż lżejsze alkany, takie jak heksan czy oktan.
Jego temperatura topnienia wynosi około –30°C, dzięki czemu w temperaturze pokojowej jest w pełni ciekły i łatwo miesza się z innymi rozpuszczalnikami organicznymi. Jako niepolarny związek, dekan nie rozpuszcza się w wodzie, ale doskonale rozpuszcza tłuszcze, oleje, parafiny, woski, niektóre polimery oraz wiele innych związków organicznych o charakterze niepolarnym lub słabo polarnym.
Inne właściwości fizyczne dekanu to:
- gęstość: około 0,73 g/cm³ (mniejsza niż woda),
- lepkość: umiarkowanie wysoka jak na węglowodór, co sprawia, że przypomina lekkie oleje,
- lotność: mniejsza niż w przypadku heksanu czy pentanu, ale nadal wyraźna,
- indeks refrakcji: około 1,41, co wpływa na jego przezroczystość i zastosowanie w analizie optycznej.
Dekan jest łatwopalny – jego temperatura zapłonu wynosi około 46°C, a więc jest niższa niż temperatura wrzenia. Opary dekanu tworzą z powietrzem mieszaniny wybuchowe, dlatego w obecności ognia, iskier czy gorących powierzchni należy zachować szczególną ostrożność. Z tego powodu dekan należy przechowywać z dala od źródeł ciepła i zapłonu, w szczelnych, wentylowanych pojemnikach.
Charakter chemiczny: nasycony węglowodór, niska reaktywność
Pod względem chemicznym dekan to klasyczny przedstawiciel nasyconych węglowodorów alifatycznych. Jego cząsteczka składa się wyłącznie z atomów węgla połączonych pojedynczymi wiązaniami, co oznacza, że wszystkie możliwe wiązania atomów węgla są nasycone atomami wodoru. Brak wiązań podwójnych, potrójnych lub grup funkcyjnych sprawia, że dekan nie bierze udziału w większości reakcji charakterystycznych dla chemii organicznej.
Reaktywność dekanu jest ograniczona, ale związek ten może uczestniczyć w kilku typowych reakcjach dla alkanów:
- spalanie – reakcja z tlenem prowadząca do powstania dwutlenku węgla i wody (przy pełnym spalaniu) lub sadzy i tlenku węgla (przy niepełnym spalaniu),
- reakcje z halogenami – np. z chlorem lub bromem, zachodzące w obecności światła UV, prowadzące do reakcji substytucji rodnikowej, w której atomy wodoru są zastępowane przez atomy halogenu,
- kraking – czyli termiczny lub katalityczny rozkład dekanu na krótsze węglowodory, często nienasycone, wykorzystywany w przemyśle petrochemicznym,
- izomeryzacja – pod wpływem katalizatorów kwasowych dekan może przekształcać się w izomery rozgałęzione o innej strukturze i właściwościach.
Ze względu na niską reaktywność i stabilność, dekan bywa wykorzystywany jako modelowy układ odniesienia w badaniach fizykochemicznych, np. do kalibracji metod chromatograficznych, pomiaru właściwości hydrofobowych, testowania polaryzacji cząsteczek lub badania oddziaływań van der Waalsa.
Cząsteczka dekanu jest także chemicznie obojętna względem większości reagentów biologicznych, co sprawia, że bywa stosowana do tworzenia warstw hydrofobowych, izolacji reakcji od wody oraz jako rozcieńczalnik dla substancji niepolarnych. W analizach spektroskopowych (np. IR lub NMR) stosuje się go jako rozpuszczalnik do substancji silnie hydrofobowych, które nie rozpuszczają się w typowych rozpuszczalnikach polarnych.
Znaczenie dekanu w chemii polega więc nie na jego aktywności reakcyjnej, lecz na jego neutralności, właściwościach fizycznych oraz zdolności do oddzielania faz i stabilizowania układów niepolarnych. To właśnie te cechy sprawiają, że mimo swojej prostoty, dekan jest niezbędnym narzędziem w laboratoriach chemicznych i przemysłowych na całym świecie.
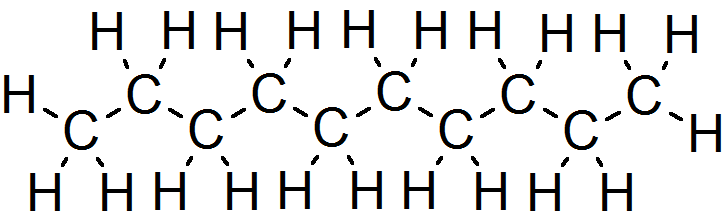
Zastosowania dekanu w przemyśle i laboratoriach
Dekan jako rozpuszczalnik organiczny
Jednym z najczęstszych zastosowań dekanu jest jego rola jako rozpuszczalnika organicznego, wykorzystywanego przede wszystkim do rozpuszczania związków hydrofobowych, czyli nierozpuszczalnych lub słabo rozpuszczalnych w wodzie. Ze względu na swoją niepolarną strukturę i brak grup funkcyjnych, dekan znakomicie rozpuszcza:
- oleje i tłuszcze,
- woski i parafiny,
- węglowodory aromatyczne,
- wiązania długołańcuchowe w chemii polimerów,
- niektóre barwniki i substancje lipofilowe.
W laboratoriach chemicznych n-dekan wykorzystywany jest jako rozcieńczalnik w badaniach spektroskopowych, szczególnie w technice FTIR, gdzie jego przezroczystość spektralna w szerokim zakresie promieniowania podczerwonego pozwala na analizę próbek bez zakłóceń tła. Ponadto jego relatywnie wysoka temperatura wrzenia sprawia, że jest stabilny w warunkach umiarkowanego podgrzewania, co czyni go przydatnym w badaniach prowadzonych w podwyższonej temperaturze.
Dekan znajduje zastosowanie także w ekstrakcjach ciecz–ciecz, gdzie dzięki niskiej mieszalności z wodą może być wykorzystywany jako faza organiczna w układach dwufazowych. W takich warunkach umożliwia oddzielanie składników mieszanin chemicznych na podstawie ich rozpuszczalności i polarności.
W niektórych procedurach chemii analitycznej i fizykochemicznej dekan służy jako modelowy rozpuszczalnik niepolarny, wykorzystywany do:
- kalibracji współczynników podziału,
- pomiaru współczynnika n-oktanowego (w standardach paliwowych),
- wyznaczania rozpuszczalności związków hydrofobowych,
- oceny właściwości transportowych w membranach organicznych.
Wykorzystanie w syntezie organicznej i analizie związków tłuszczowych
Dekan jest ceniony w syntezie organicznej jako rozpuszczalnik obojętny – nie wchodzi w reakcje z większością reagentów organicznych i nie zakłóca działania katalizatorów ani związków funkcyjnych. Znajduje zastosowanie przede wszystkim w reakcjach:
- prowadzonych w środowisku beztlenowym (inertnym),
- z udziałem związków wrażliwych na wodę lub tlen,
- wymagających wysokich temperatur, przy zachowaniu stabilnego rozpuszczalnika,
- testujących hydrofobowość produktów, np. przy syntezie związków powierzchniowo czynnych.
W badaniach nad związkami lipidowymi, olejami naturalnymi i estrami kwasów tłuszczowych, dekan pełni funkcję rozpuszczalnika wzorcowego. Jest także wykorzystywany do rozcieńczania prób do badań metodami GC (chromatografii gazowej), gdzie jego niska lotność i obojętność pozwalają uniknąć zakłóceń analitycznych.
W przemyśle petrochemicznym i rafineryjnym n-dekan wykorzystywany jest również jako składnik mieszanek paliwowych i standardów kalibracyjnych, ponieważ jego obecność w próbce paliwa może posłużyć do kalibracji przyrządów pomiarowych oraz wyznaczania właściwości fizykochemicznych takich jak:
- liczba cetanowa,
- temperatura zapłonu,
- lepkość,
- charakterystyka parowania.
Dekan bywa także składnikiem syntetycznych olejów bazowych, używanych w przemyśle motoryzacyjnym i maszynowym, a jego obecność wpływa na zwiększenie smarowności, lepkości i odporności chemicznej produktów końcowych.
Rola dekanu w modelach chemicznych i badaniach hydrofobowości
Dzięki swojej niepolarniej naturze i wyraźnie hydrofobowemu charakterowi, dekan znajduje szerokie zastosowanie w badaniach naukowych dotyczących interakcji między cząsteczkami, właściwości powierzchniowych oraz transportu substancji w układach biologicznych i technicznych.
W badaniach akademickich i przemysłowych dekan pełni rolę:
- modelowej substancji hydrofobowej, w testach oddziaływań z białkami, membranami i powierzchniami polimerowymi,
- medium referencyjnego w ocenie hydrofobowości powierzchni, m.in. przez pomiar kąta zwilżania,
- fazy olejowej w układach mikroemulsyjnych,
- rozpuszczalnika do testowania sorbentów, np. aktywowanych węgli i zeolitów pod kątem zdolności adsorpcji niepolarnych substancji.
W biotechnologii i biofizyce dekan może być stosowany jako sztuczne środowisko lipidowe do modelowania błon komórkowych, gdzie jego właściwości fizykochemiczne pozwalają ocenić zachowanie związków biologicznych w warunkach niskiej polarności – takich jak wewnętrzne warstwy błon biologicznych.
Dekan wykorzystywany jest także w badaniach nad nowoczesnymi materiałami izolacyjnymi, powlokami hydrofobowymi oraz strukturami samoorganizującymi się, gdzie pełni funkcję nośnika, środowiska reakcyjnego lub medium kalibracyjnego.
Dzięki swojej obojętności chemicznej, wysokiej czystości handlowej i przewidywalnym właściwościom fizycznym, dekan jest powszechnie stosowany nie tylko w przemyśle, ale również w nauce eksperymentalnej, stanowiąc jeden z najlepiej zdefiniowanych i opisanych rozpuszczalników niepolarnych w chemii nowoczesnej.
Bezpieczeństwo, przechowywanie i wpływ na środowisko
Potencjalne zagrożenia przy pracy z dekanem
Dekan, mimo że należy do związków chemicznych o niskiej toksyczności ostrej, wymaga przestrzegania podstawowych zasad bezpieczeństwa podczas użytkowania, zwłaszcza w warunkach laboratoryjnych i przemysłowych. Jego opary mogą działać drażniąco na układ oddechowy, a kontakt cieczy ze skórą lub oczami może wywołać podrażnienie, zaczerwienienie i uczucie pieczenia. Ze względu na swoje właściwości fizykochemiczne, dekan jest również łatwopalny – tworzy z powietrzem mieszaniny wybuchowe, szczególnie w zamkniętych i słabo wentylowanych pomieszczeniach.
Główne zagrożenia związane z użytkowaniem dekanu obejmują:
- ryzyko pożaru lub eksplozji w obecności otwartego ognia, iskier lub gorących powierzchni,
- działanie drażniące oparów na oczy, gardło i drogi oddechowe,
- efekt odtłuszczający na skórę, prowadzący przy dłuższym kontakcie do jej wysuszenia i mikrouszkodzeń,
- możliwość wdychania oparów przy pracy bez odpowiedniej wentylacji, co w wysokim stężeniu może powodować bóle głowy, zawroty, senność, a nawet zaburzenia koordynacji ruchowej.
Podczas pracy z dekanem należy zawsze:
- stosować rękawice nitrylowe lub neoprenowe,
- nosić okulary ochronne lub przyłbicę,
- zapewnić dobrą wentylację lub pracować w dygestorium,
- unikać stosowania urządzeń elektrycznych bez zabezpieczeń przeciwwybuchowych,
- nie jeść, nie pić i nie palić w pobliżu stanowiska pracy.
W razie rozlania większej ilości dekanu, należy natychmiast zneutralizować go materiałem chłonnym (np. piaskiem, ziemią okrzemkową), zebrać do szczelnych pojemników i przekazać do utylizacji zgodnie z przepisami. Miejsce rozlania należy przewietrzyć i przemyć wodą z detergentem. Nigdy nie należy dopuścić do spływania dekanu do kanalizacji lub cieków wodnych.
Zasady przechowywania i etykietowania
Aby zminimalizować ryzyko związane z przechowywaniem, dekan powinien być trzymany w szczelnie zamkniętych pojemnikach, wykonanych z materiałów odpornych na działanie węglowodorów, takich jak szkło borokrzemowe lub tworzywa sztuczne o wysokiej odporności chemicznej (np. HDPE). Butelki powinny być przechowywane:
- w chłodnym, dobrze wentylowanym miejscu,
- z dala od źródeł zapłonu, promieniowania słonecznego i wysokich temperatur,
- w magazynach substancji łatwopalnych, oznaczonych zgodnie z przepisami BHP.
Etykieta na opakowaniu z dekanem powinna zawierać:
- nazwę chemiczną: n-dekan lub dekan (C₁₀H₂₂),
- piktogram GHS: płomień (łatwopalny) oraz wykrzyknik (substancja drażniąca),
- zwroty H i P: np. H226 – Łatwopalna ciecz i pary, H336 – Może wywoływać senność i zawroty głowy, P210 – Przechowywać z dala od źródeł ciepła,
- numer CAS: 124-18-5.
Dekan nie wymaga przechowywania w warunkach chłodniczych, ale długoterminowe utrzymywanie go w temperaturze poniżej 25°C zwiększa jego stabilność i ogranicza parowanie. Roztwory z dekanem przygotowywane w laboratorium należy oznaczać datą sporządzenia i wykorzystywać w możliwie krótkim czasie, aby uniknąć degradacji lub zanieczyszczeń.
Dekan jako związek o niskiej biodegradowalności
Z chemicznego punktu widzenia dekan jest bardzo trwałym związkiem organicznym, co sprawia, że ulega bardzo wolnej biodegradacji w środowisku naturalnym. Ze względu na swoją niepolarną strukturę oraz niską rozpuszczalność w wodzie, dekan:
- łatwo adsorbuje się na cząstkach gleby,
- tworzy cienkie warstwy na powierzchni wód,
- utrudnia wymianę gazową między wodą a atmosferą,
- może bioakumulować się w tkankach organizmów wodnych, jeśli obecny jest w dużych ilościach.
W środowisku wodnym dekan rozkłada się wyłącznie w obecności wyspecjalizowanych mikroorganizmów, które potrafią rozszczepiać wiązania C–C i wprowadzać tlen do cząsteczki węglowodoru. Proces ten jest powolny i mało wydajny, szczególnie w warunkach beztlenowych. Dlatego niekontrolowane uwalnianie dekanu do środowiska (np. przez zrzuty przemysłowe lub wylewy magazynowe) może powodować:
- długotrwałe zanieczyszczenie gleby i wód,
- toksyczne działanie na mikroorganizmy i plankton,
- zaburzenia w łańcuchach pokarmowych wodnych ekosystemów.
Z tego względu dekan należy utylizować jako odpad niebezpieczny, zgodnie z przepisami prawa lokalnego i unijnego. Odpady ciekłe zawierające dekan powinny trafiać do specjalistycznych instalacji utylizacyjnych, które przeprowadzają termiczne spalanie z odzyskiem energii lub bezpieczną neutralizację chemiczną.
Warto dodać, że dekan – podobnie jak inne alkany długołańcuchowe – nie jest klasyfikowany jako związek szczególnie toksyczny, ale jego obecność w środowisku w dużych ilościach może prowadzić do długoterminowych, trudnych do odwrócenia skutków ekologicznych, szczególnie w ekosystemach wodnych.
Dlatego odpowiedzialne stosowanie, przechowywanie i utylizacja dekanu to nie tylko obowiązek prawny, ale również element dobrej praktyki laboratoryjnej i przemysłowej, który wpisuje się w nowoczesne podejście do ochrony środowiska. Właściwe zarządzanie tą substancją pozwala korzystać z jej cennych właściwości bez narażania ludzi ani przyrody na zbędne ryzyko.
FAQ dekan – właściwości, zastosowanie i bezpieczeństwo
Co to jest dekan?
Dekan to nasycony węglowodór o wzorze chemicznym C10H22, należący do grupy alkanów, występujący w postaci bezbarwnej cieczy o charakterystycznym zapachu.
Jakie właściwości fizyczne ma dekan?
Dekan ma temperaturę wrzenia około 174°C, jest nierozpuszczalny w wodzie, dobrze rozpuszcza tłuszcze i inne związki organiczne, oraz jest łatwopalny.
Do czego używa się dekanu?
Dekan jest wykorzystywany jako rozpuszczalnik w laboratoriach, nośnik w reakcjach organicznych, oraz modelowy związek w badaniach właściwości hydrofobowych.
Czy dekan jest bezpieczny?
W niewielkich ilościach jest mało toksyczny, ale jego opary mogą działać drażniąco; należy unikać wdychania i kontaktu ze skórą, a także przechowywać go z dala od źródeł ognia.
Jak wpływa dekan na środowisko?
Dekan ulega powolnej biodegradacji, może zanieczyszczać wody i gleby, dlatego należy go utylizować zgodnie z zasadami ochrony środowiska.
- Lamele ścienne – praktyczny i estetyczny materiał do nowoczesnych aranżacji wnętrz - 30 października, 2025
- Jak wybrać idealny sweter męski rozpinany? 4 wskazówki - 1 października, 2025
- BREEAM – praktyczny przewodnik po certyfikacji zrównoważonych budynków - 24 września, 2025




Opublikuj komentarz