Co to jest tlenek fosforu 5 i jaka jest jego budowa chemiczna
Wzór sumaryczny i nazewnictwo: P₂O₅ a P₄O₁₀
Tlenek fosforu 5, znany również jako tlenek fosforowy(V), to nieorganiczny związek chemiczny fosforu i tlenu, w którym fosfor występuje na najwyższym stopniu utlenienia, czyli +5. Jego powszechnie stosowany wzór sumaryczny to P₂O₅, jednak w rzeczywistości nie występuje on w tej formie jako pojedyncza cząsteczka.
Prawidłowy wzór strukturalny cząsteczki to P₄O₁₀, co oznacza, że rzeczywista postać tlenku fosforu 5 to tetramer, czyli związek złożony z czterech atomów fosforu i dziesięciu atomów tlenu. Forma P₂O₅ jest stosowana dla wygody i tradycyjnie przyjęta jako „empiryczny” wzór opisujący stosunek atomów, natomiast P₄O₁₀ jest wzorem cząsteczkowym opisującym rzeczywistą strukturę.
Z chemicznego punktu widzenia tlenek fosforu 5 jest beztlenkowym kwasem tlenowym, który w kontakcie z wodą tworzy kwas fosforowy (H₃PO₄). To sprawia, że P₂O₅ zalicza się do tlenków kwasowych, podobnie jak SO₃ czy CO₂.
Struktura cząsteczki i właściwości fizyczne
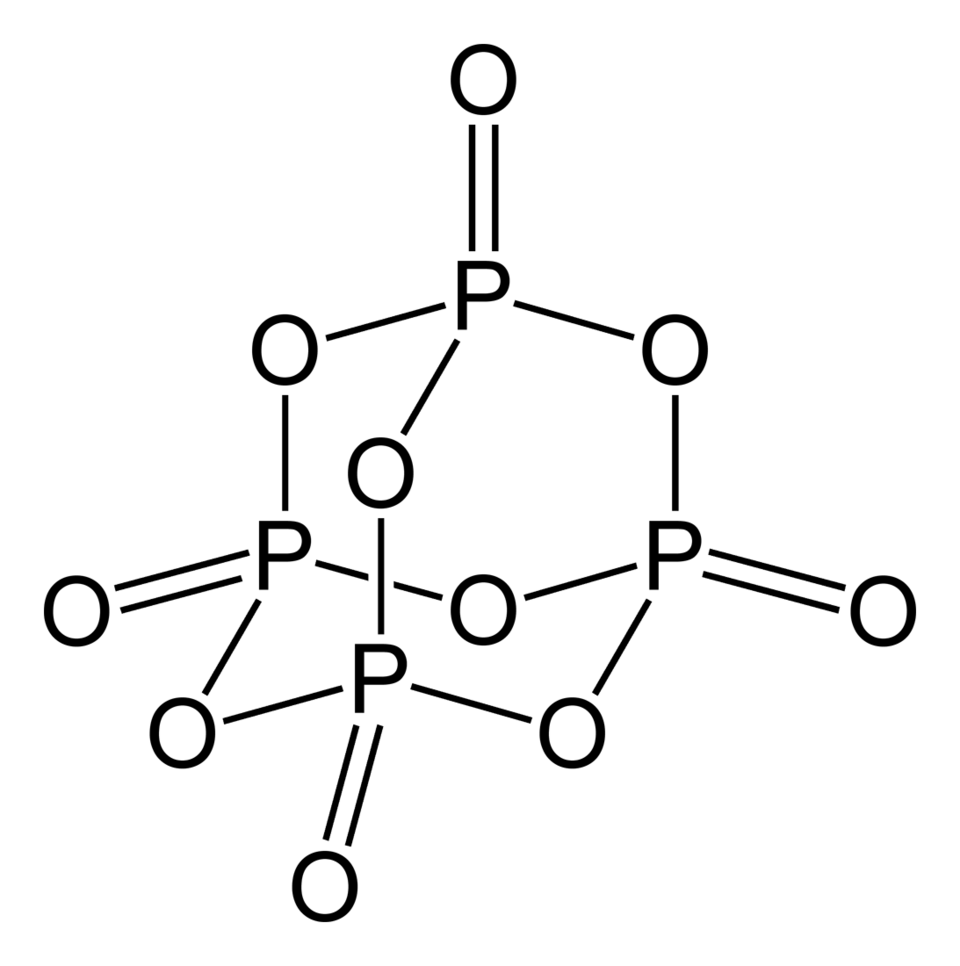
Cząsteczka P₄O₁₀ ma dość złożoną strukturę trójwymiarową, wynikającą z tetraedrycznego układu atomów fosforu. Każdy atom fosforu jest połączony z czterema atomami tlenu: trzema mostkowymi (łączącymi dwa atomy P) i jednym tlenem końcowym (dwuatomowym wiązaniem P=O). W rezultacie otrzymujemy strukturę, w której:
- atomy fosforu tworzą centralny czworościan,
- każdy atom P ma cztery atomy tlenu jako ligandy,
- tlenki mostkowe łączą sąsiednie atomy P, nadając całej cząsteczce charakter pierścieniowy lub klatkowy.
Taka struktura zapewnia cząsteczce dużą stabilność i wysoką reaktywność chemiczną jednocześnie – czyni ją doskonałym środkiem wiążącym wodę oraz tlen.
Fizycznie tlenek fosforu 5 to:
- biały, krystaliczny proszek lub szklista masa (w zależności od metody otrzymywania),
- bardzo silnie higroskopijny, co oznacza, że intensywnie pochłania wodę z otoczenia – do tego stopnia, że może osuszać powietrze i niszczyć naczynia laboratoryjne wykonane z tworzyw sztucznych,
- bez zapachu, ale jego pył może drażnić drogi oddechowe i oczy,
- topi się w temperaturze ok. 340°C, a przy dalszym ogrzewaniu ulega sublimacji.
Ważną właściwością P₄O₁₀ jest jego reakcja z wodą, którą omówimy w kolejnej części – reakcja ta jest tak silna, że często wykorzystywana jest do usuwania wody z substancji chemicznych, zarówno w laboratoriach, jak i w przemyśle.
Powstawanie tlenku fosforu(V) w reakcji spalania fosforu
Tlenek fosforu 5 można uzyskać w warunkach laboratoryjnych lub przemysłowych w sposób stosunkowo prosty – poprzez spalanie fosforu w nadmiarze tlenu. Reakcja ta przebiega gwałtownie i egzotermicznie, z wydzieleniem dużej ilości ciepła i charakterystycznym białym dymem tlenku:
4P + 5O₂ → 2P₂O₅
Reakcja ta zachodzi intensywnie, dlatego do jej przeprowadzenia potrzebne są odpowiednie zabezpieczenia – unika się wykonywania jej w otwartych naczyniach laboratoryjnych. W przemyśle stosuje się kontrolowane spalanie żółtego fosforu w komorach tlenowych, a powstający P₄O₁₀ jest następnie kondensowany i oczyszczany.
Istnieją również metody otrzymywania tlenku fosforu 5 z użyciem bardziej zaawansowanych technik, takich jak:
- utlenianie związków fosforu (np. fosforanów) w atmosferze tlenu,
- reakcje redoks z silnymi utleniaczami w obecności suszących środków katalitycznych.
Niezależnie od metody, powstały związek musi być przechowywany w szczelnie zamkniętych pojemnikach, ponieważ już krótki kontakt z wilgocią z powietrza prowadzi do jego szybkiej hydrolizy.
Dzięki tym właściwościom tlenek fosforu 5 zaliczany jest do najsilniejszych znanych środków odwadniających. Jego struktura molekularna i wysoka reaktywność wobec wody sprawiają, że nie tylko pochłania parę wodną, ale chemicznie wiąże cząsteczki H₂O, przechodząc w kwas fosforowy lub jego polikondensaty.
Tlenek fosforu 5 to klasyczny przykład tlenku kwasowego, który dzięki swojej specyficznej strukturze i silnemu powinowactwu do wody odgrywa ważną rolę w wielu gałęziach przemysłu chemicznego. W kolejnej części przyjrzymy się szczegółowo jego właściwościom chemicznym oraz reakcjom z wodą, zasadami i związkami organicznymi.
Właściwości chemiczne tlenku fosforu 5 i jego reakcje z wodą
Silne właściwości higroskopijne i reakcja z wodą
Tlenek fosforu 5 (P₂O₅) wyróżnia się jedną z najbardziej wyrazistych cech spośród tlenków kwasowych – jest silnie higroskopijny, czyli ma wyjątkową zdolność pochłaniania wilgoci z powietrza. Jednak nie ogranicza się on jedynie do pasywnego wiązania cząsteczek wody – jego działanie jest chemicznie aktywne.
W kontakcie z wodą zachodzi gwałtowna, silnie egzotermiczna reakcja, w której P₂O₅ przekształca się w kwas fosforowy(V) (H₃PO₄). Proces ten zachodzi według równania:
P₄O₁₀ + 6H₂O → 4H₃PO₄
Oznacza to, że jedna cząsteczka tlenku fosforu 5 reaguje z sześcioma cząsteczkami wody, tworząc cztery cząsteczki kwasu fosforowego. Reakcja ta zachodzi z wydzieleniem dużej ilości ciepła – w praktyce, przy dodawaniu P₂O₅ do wody, może dojść do wrzenia mieszaniny i jej rozprysków, dlatego należy ją prowadzić bardzo ostrożnie.
Właściwość ta sprawia, że P₂O₅ jest powszechnie wykorzystywany jako środek odwadniający, m.in. do:
- suszenia gazów (np. powietrza, amoniaku),
- usuwania wody z organicznych roztworów,
- przygotowywania próbek bezwodnych w analizie instrumentalnej,
- tworzenia warunków bezwodnych w reakcjach organicznych.
O jego sile jako dehydratora świadczy fakt, że jest zdolny do:
- usuńcia wody związanej chemicznie,
- rozkładania hydratów,
- przekształcania kwasów do ich bezwodników, np. HNO₃ → N₂O₅.
Tworzenie kwasu fosforowego(V) – H₃PO₄
Reakcja z wodą prowadzi do powstania kwasu ortofosforowego, znanego również jako kwas fosforowy(V). Powstały kwas H₃PO₄ jest cieczą o wysokiej lepkości, nietoksyczną w umiarkowanych stężeniach i szeroko wykorzystywaną w przemyśle spożywczym (np. jako regulator kwasowości w napojach gazowanych) i nawozowym.
Przy niedostatecznej ilości wody, zamiast w pełni uwodnionego kwasu, powstają jego polifosforanowe formy pośrednie, np.:
- kwas pirofosforowy (H₄P₂O₇),
- kwas metafosforowy ((HPO₃)ₙ),
- polikwas fosforowy – forma zawierająca wiele połączonych jednostek PO₄.
Reakcja z wodą może być kontrolowana w warunkach laboratoryjnych, aby uzyskać odpowiednią formę kwasu – co ma duże znaczenie w procesach technologicznych i syntezie nawozów sztucznych.
Reaktywność wobec zasad, alkoholi i substancji organicznych
Tlenek fosforu 5, będąc tlenkiem kwasowym, reaguje chętnie z zasadami, tworząc fosforany. Przykładowo, reakcja z wodorotlenkiem sodu prowadzi do powstania fosforanu sodu:
P₂O₅ + 6NaOH → 2Na₃PO₄ + 3H₂O
Takie reakcje wykorzystywane są w syntezie soli fosforanowych, które mają szerokie zastosowanie w:
- przemyśle spożywczym (regulatory kwasowości),
- produkcji detergentów (choć ograniczanej ze względu na eutrofizację wód),
- tworzeniu nawozów mineralnych (fosforany jednosodowe, disodowe, trisodowe).
Oprócz reakcji z zasadami, P₂O₅ wykazuje silne właściwości kondensujące – co oznacza, że potrafi usuwać wodę z cząsteczek organicznych, prowadząc do ich cyklizacji, odwodnienia lub powstania bezwodników. W związku z tym jest szeroko stosowany w syntezie organicznej, np. do:
- przekształcania amidów w nitryle,
- odwodnienia alkoholi do alkenów,
- tworzenia bezwodników kwasowych z kwasów karboksylowych,
- syntezy fosforynów i estrów fosforanowych.
Reakcja ta jest bardzo przydatna, gdyż często nie wymaga rozpuszczalników i może być przeprowadzana w warunkach łagodnych, z wysoką selektywnością. Dodatkowo, P₂O₅ często stosuje się w chemii preparatywnej jako czynnik końcowego osuszenia – usuwania ostatnich śladów wilgoci z produktu, np. po ekstrakcji lub krystalizacji.
Tlenek fosforu 5 ma też zdolność do niszczenia struktur bogatych w grupy hydroksylowe, dlatego nie powinien mieć kontaktu z papierem, drewnem czy tkaninami zawierającymi celulozę – może doprowadzić do ich kruszenia i rozpadu.
Reaktywność chemiczna P₂O₅ wynika z jego silnego powinowactwa do wody oraz zdolności do tworzenia trwałych struktur zawierających wiązania P=O i P–O–P. Z tego względu jest to związek nie tylko teoretycznie interesujący, ale również praktycznie niezbędny w wielu gałęziach przemysłu i laboratoriów chemicznych. W kolejnej części omówimy, gdzie dokładnie znajduje zastosowanie – od nawozów po syntezę leków.

Praktyczne zastosowania P₂O₅ w przemyśle i laboratoriach
Tlenek fosforu 5 jako środek suszący i odwadniający
Jednym z najbardziej znanych i cenionych zastosowań tlenku fosforu 5 (P₂O₅) jest jego rola jako bardzo silny środek odwadniający. Działa on znacznie skuteczniej niż tradycyjne suszarki chemiczne, takie jak chlorek wapnia czy siarczan magnezu. Jego wyjątkowa aktywność wynika z ogromnego powinowactwa do wody, co pozwala mu:
- wiązać cząsteczki wody zawarte w gazach i cieczach,
- usuwać wilgoć z reagentów i próbek,
- tworzyć trwałe połączenia z wodą, prowadzące do powstania kwasu fosforowego lub jego pochodnych.
P₂O₅ stosuje się do suszenia:
- substancji organicznych, które nie mogą być ogrzewane,
- roztworów rozpuszczalników, takich jak eter dietylowy, chloroform czy acetonitril,
- powietrza i innych gazów w analizatorach, kolumnach chromatograficznych i systemach optycznych.
Jest niezastąpiony w sytuacjach, gdzie wymagane są warunki bezwodne – np. przy pracy z reagentami wrażliwymi na wodę, w syntezie Grignarda, reakcji z wodorkami metali czy związkami litoorganicznymi. Dzięki temu znalazł trwałe miejsce w każdej dobrze wyposażonej pracowni chemicznej.
W praktyce P₂O₅ umieszcza się w eksykatorach, kolumnach suszących lub w odpowiednio zabezpieczonych naczyniach. Jego użycie wymaga jednak ostrożności – ze względu na silne działanie egzotermiczne w kontakcie z wodą i możliwość uszkodzenia tkanek.
Zastosowanie w produkcji kwasu fosforowego i nawozów
Kwas fosforowy (H₃PO₄), powstający w reakcji tlenku fosforu 5 z wodą, jest jednym z najważniejszych produktów chemicznych na świecie. To właśnie z P₂O₅ uzyskuje się jego najczystszą formę – tzw. kwas fosforowy bezpośredni, stosowany m.in. w:
- produkcji wysokiej klasy nawozów mineralnych,
- żywności i napojach (regulator kwasowości E338),
- przemysłowej produkcji detergentów, płynów do mycia i środków czyszczących,
- przetwórstwie metali – trawienie powierzchni i ochrona przed korozją,
- preparatach farmaceutycznych i stomatologicznych.
W przemyśle nawozowym kwas fosforowy jest używany do produkcji:
- fosforanu jednowapniowego (Ca(H₂PO₄)₂) – dodawanego do pasz zwierzęcych,
- superfosfatów – nawozów poprawiających wzrost i rozwój systemów korzeniowych,
- fosforanów potasu i amonu – składników kompleksowych nawozów wieloskładnikowych.
Choć na skalę przemysłową P₂O₅ nie jest zawsze używany jako surowiec wyjściowy (często stosuje się bezpośrednie ługowanie fosforytów kwasem siarkowym), jego zastosowanie ma znaczenie w produkcji czystego, laboratoryjnego kwasu fosforowego, wolnego od domieszek i metali ciężkich.
Użycie w syntezie organicznej i preparatyce chemicznej
W chemii organicznej i technologiach syntezy związków specjalistycznych, tlenek fosforu 5 pełni rolę nie tylko suszarki, ale przede wszystkim reagenta kondensującego, który:
- usuwa cząsteczki wody z reakcji kondensacji, przesuwając równowagę w stronę produktów,
- umożliwia cyklizację i tworzenie wiązań wielokrotnych,
- katalizuje tworzenie bezwodników, estrów i związków fosforowych.
Typowe reakcje z udziałem P₂O₅ to:
- odwodnienie alkoholi do alkenów,
- przekształcenie amidów w nitryle (reakcja dehydratacyjna),
- synteza bezwodników kwasowych z kwasów karboksylowych,
- tworzenie estrów fosforanowych wykorzystywanych w biochemii i chemii leków.
Dzięki temu P₂O₅ jest nieodzowny w:
- laboratoriach farmaceutycznych – np. przy syntezie prekursorów leków przeciwwirusowych i przeciwzapalnych,
- chemii materiałowej – np. przy opracowywaniu polimerów przewodzących,
- przemyśle spożywczym – np. do produkcji dodatków fosforanowych.
Oprócz zastosowań stricte laboratoryjnych, P₂O₅ znajduje się też w składzie niektórych specjalistycznych preparatów do usuwania wilgoci, regeneracji katalizatorów, oczyszczania gazów przemysłowych oraz jako składnik substancji chemicznych do zaawansowanego trawienia fotolitograficznego w mikroelektronice.
Jego unikalna zdolność do reagowania z wodą – nie tylko fizycznie, ale i chemicznie – sprawia, że trudno znaleźć dla niego równie skuteczny zamiennik. Dzięki wysokiej skuteczności i szerokiemu zakresowi reakcji, tlenek fosforu 5 pozostaje jednym z najbardziej uniwersalnych i użytecznych związków chemicznych, zarówno w pracy naukowców, jak i w ogromnych zakładach przemysłowych. Bez niego nie byłoby wielu kluczowych technologii i produktów, które dziś traktujemy jako oczywistość.
FAQ tlenek fosforu 5 – najczęstsze pytania i odpowiedzi
Jaki jest wzór tlenku fosforu 5?
Wzór sumaryczny to P₂O₅, ale rzeczywista cząsteczka ma postać P₄O₁₀, ponieważ fosfor występuje w cząsteczkach tetramerycznych.
Jak powstaje tlenek fosforu 5?
Powstaje w wyniku spalania fosforu w nadmiarze tlenu: 4P + 5O₂ → 2P₂O₅.
Jakie są właściwości fizyczne P₂O₅?
To biały, krystaliczny, silnie higroskopijny proszek, który w kontakcie z wodą tworzy kwas fosforowy.
Do czego służy tlenek fosforu 5?
Jest stosowany jako środek odwadniający, w produkcji kwasu fosforowego, nawozów i jako reagent w chemii organicznej.
Czy P₂O₅ jest niebezpieczny?
Tak, działa drażniąco na skórę, oczy i drogi oddechowe, a jego reakcja z wodą jest silnie egzotermiczna – należy obchodzić się z nim ostrożnie.







